
Yutaro Ibi, Koichiro Miike, Tomoko Ohmori, Chen-Leng Cai, Shunsuke Tanigawa, Ryuichi Nishinakamura. In vitro generation of a ureteral organoid from pluripotent stem cells. Nature Communications, 16: 5309, 2025.
https://doi.org/10.1038/s41467-025-60693-6
[概要説明]
尿管は腎臓で生成された尿の出口を構成し、腎臓が機能を果たすために必須の臓器です。尿管は上皮とそれを取り囲む間質で構成されており、これらの前駆細胞が相互作用を繰り返し発生します。この2つの構成組織のうち尿管上皮の前駆細胞 (尿管芽) を多能性幹細胞 (マウスES細胞やヒトiPS細胞) から人為的に誘導する方法は、熊本大学発生医学研究所の腎臓発生分野 (西中村隆一教授) をはじめ複数報告されていましたが、尿管間質の前駆細胞を誘導する方法は世界的に見ても確立されていませんでした。今回、同グループの伊比裕太郎大学院生らは、この尿管間質の前駆細胞を多能性幹細胞から誘導する方法を開発しました。さらに誘導した尿管間質前駆細胞を、マウス胎仔由来の尿管上皮や多能性幹細胞から誘導した尿管芽と組み合わせることで、人工的に尿管組織 (尿管オルガノイド) を再構成することに成功しました。
本研究は、尿管という腎臓からの尿排泄に必須となる構造を試験管内で多能性幹細胞から構築することに成功した初めての報告です。この技術を腎臓オルガノイドと組み合わせれば、尿が作られて出ていくという臓器本来の機能を持った移植用の腎臓を作るという次世代の再生医療に向け大きな前進となります。また、尿管疾患の病態解明と創薬開発に繋がることも期待されます。
本研究成果は、科学雑誌「Nature Communications」のオンライン版に6月20日に掲載されました。本研究は、文部科学省科学研究費補助金(基盤研究(S))、国際先導研究「腎臓を創る」、JST創発的研究支援事業の支援を受けました。
[背景]
腎臓は人体の恒常性維持を担う重要な臓器ですが、再生しない臓器です。腎不全による人工透析患者さんは日本国内だけでも34万人を超えており、腎移植の機会も限られていることから腎臓の再生医療に期待が集まっています。
近年の幹細胞生物学の進歩により、多能性幹細胞から腎臓組織を人工的に作ることが可能になっています。熊本大学発生医学研究所腎臓発生分野はこれまで、多能性幹細胞から腎臓を構成する前駆細胞の誘導法を世界に先駆けて確立し、特にマウスES細胞から複雑な三次元構造(高次構造)を有する腎臓組織 (腎臓オルガノイド) を作ることに成功しました (Cell Stem Cell 2014 & 2017, Nat Commun 2022)。しかしこの腎臓組織には産生された尿の排泄経路である「尿管」は付随しておらず、このことが腎臓オルガノイドを移植医療に応用する際のボトルネックになっています。
尿管は上皮と間質で構成され、これらの前駆細胞の相互作用により発生します。これらのうち尿管上皮の前駆細胞 (尿管芽) への誘導法は、同グループを含め (Cell Stem Cell 2017) 複数報告されていますが、残る尿管間質の前駆細胞への誘導法は世界的にみても確立されていませんでした。今回は、この尿管間質の前駆細胞を多能性幹細胞から誘導する方法を確立し、マウス胎仔由来の尿管上皮、もしくは多能性幹細胞から誘導した尿管芽と組み合わせることで、多能性幹細胞から尿管組織を作ることを目的としました。
[研究の内容]
まず胎児期のマウス腎臓、尿管を用いて、尿管間質の前駆細胞に特徴的な遺伝子群やその発生メカニズムを同定しました。次に、尿管間質の前駆細胞の起源である後方中間中胚葉と呼ばれる組織を単離し、それを尿管間質の前駆細胞まで誘導する培養条件を確立しました。これらを基に、マウスES細胞とヒトiPS細胞から後方中間中胚葉を経由して尿管間質の前駆細胞を誘導する方法を開発しました。この誘導した尿管間質の前駆細胞を、マウス胎仔由来の尿管上皮や多能性幹細胞から誘導した尿管芽と組み合わせて試験管内で培養し、分化した尿管組織を作ることに成功しました(図)。さらにこれらの方法は、尿管に異常をきたす遺伝子の機能解明に利用できることも示しました。
[成果・展開]
本研究は、尿管間質の前駆細胞の誘導法を確立し、生体内の尿管上皮や誘導した尿管芽と組み合わせることで、人工的な尿管組織の作成を実現したものです。尿管という生体内で腎臓が機能を発揮するために必須な構造を、試験管内で多能性幹細胞から構築することに成功した初めての報告であり、尿管に異常がみられる様々な疾患の病態解明に応用が可能です。また、すでに同グループから発表済みである、高次構造を有する腎臓オルガノイドと繋ぎ合わせることができれば、尿が作られて出ていくという臓器本来の機能を持った腎臓オルガノイドを試験管内で作って移植できるようになる可能性があります。今後のステップとして、尿管オルガノイドの質を高め、腎臓オルガノイドに繋げる研究が期待されます。
[用語解説]
・尿管:腎臓で産生される尿を体外に排泄するために必要な構造。管状の構造をしており、内側に位置する上皮とそれを取り囲む間質で構成される。
・多能性幹細胞:ES細胞やiPS細胞など。様々な体細胞に分化し得る万能細胞。
・ES細胞:受精卵から作られた多能性幹細胞。胚性幹細胞。
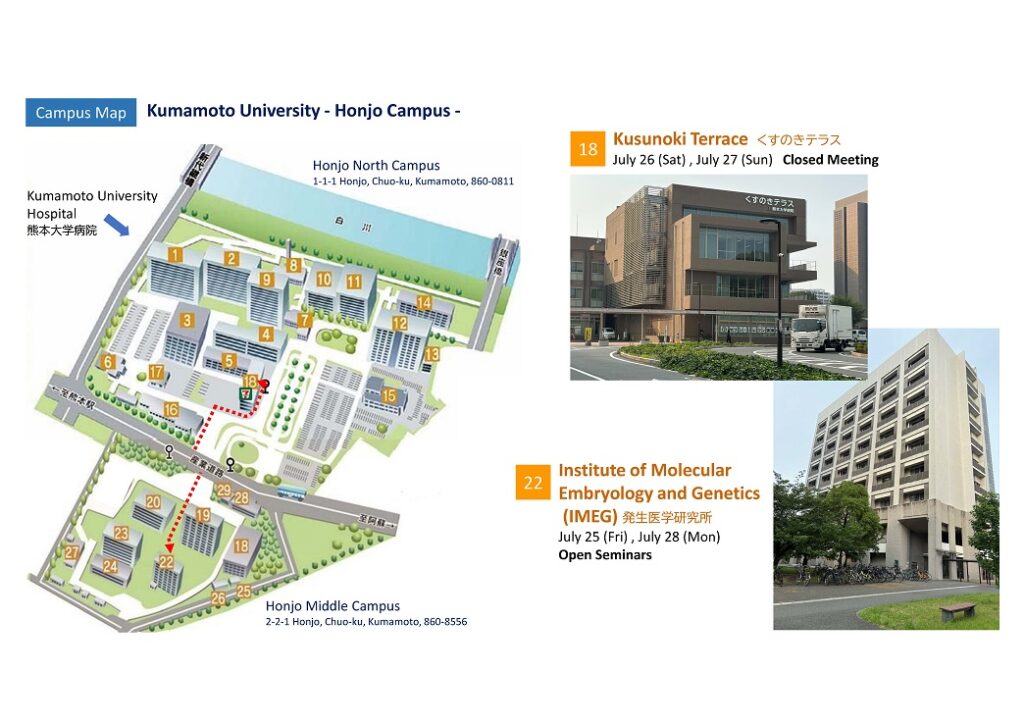
・iPS細胞:皮膚や血液などの体細胞から作られた多能性幹細胞。
・尿管芽:尿管上皮の前駆細胞。腎臓内の構造の一部でもある集合管の前駆細胞でもある。
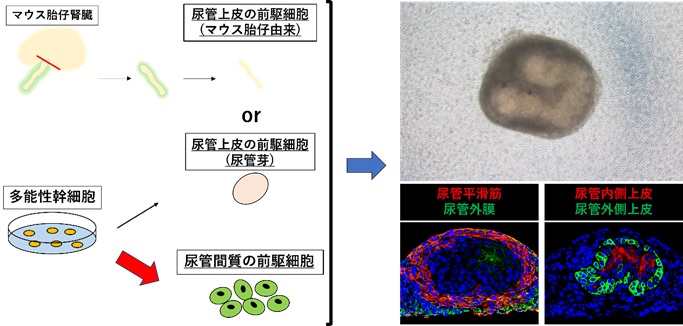
[図の説明]
多能性幹細胞から尿管間質の前駆細胞への誘導法を開発し(赤矢印)、マウス胎仔由来、もしくは多能性幹細胞から誘導した尿管上皮の前駆細胞と組み合わせることで人工的に尿管組織を作ることに成功した(写真上段:マウスES細胞由来の尿管間質前駆細胞とマウス胎仔由来の尿管上皮を組み合わせた尿管組織を示す)。作製した尿管組織は生体内の尿管と同様に分化していることが確認できた(写真下段、作製した尿管組織の断面を示す)。
国内から29名、海外から3名が参加して第3回webミーティングが行われました。理化学研究所の尾藤和浩さん(国際先導研究リサーチアソシエイト)が最新の研究成果を発表し、活発な議論がなされました。
We usually have a meeting on the second Tuesday of the month.
(Japan time)
Apr 8 Nishinakamura
May 13 Yokoo
June 17 Takasato (3rd Tuesday to avoid overlap with ISSCR)
July no Zoom meeting (Kumamoto Retreat on July 26-27)
Aug no Zoom meeting
Sep 9 Yokokawa
Oct 14 Tanigawa
Nov 11 Nishinakamura
Dec 9 Yokoo
Jan 13 Takasato
Feb 10 Yokokawa
Mar 10 Tanigawa
国内から24名、海外から3名が参加して第2回webミーティングが行われました。ワシントン大学セントルイス校の松井賢治さん(国際先導研究研究員)が慈恵医大在籍時の研究成果を発表し、活発な議論がなされました。
We usually have a meeting on the second Tuesday of the month.
(Japan time)
Apr 8 Nishinakamura
May 13 Yokoo
June 17 Takasato (3rd Tuesday to avoid overlap with ISSCR)
July no Zoom meeting (Kumamoto Retreat on July 26-27)
Aug no Zoom meeting
Sep 9 Yokokawa
Oct 14 Tanigawa
Nov 11 Nishinakamura
Dec 9 Yokoo
Jan 13 Takasato
Feb 10 Yokokawa
Mar 10 Tanigawa
ヒトiPS細胞由来腎臓オルガノイドを用いた近位尿細管モデルを開発
~薬物輸送体の機能解析と腎毒性評価のためのMicrophysiological systems (MPS)~
Summary:
We present a protocol for generating a proximal tubule-on-chip using hiPSC-derived kidney organoids. It includes organoid differentiation, proximal tubule cell isolation, and seeding on a chip, enabling enhanced transporter expression. The model supports evaluations of substrate transport by renal transporters, nephrotoxicity, and drug interactions.
本論文は、hiPSC由来の腎臓オルガノイドを用いて近位尿細管の生体模倣システム(Microphysiological systems (MPS))を作製するプロトコルを説明したものである。このプロトコルを用いると、オルガノイドの分化誘導、近位尿細管上皮細胞の単離、チップへの播種を通してトランスポーターの発現量が向上する。このモデルを用いて、腎トランスポーターによる基質輸送能、腎毒性、薬物相互作用等を評価することができた。
Affiliations of all co-researchers:
Ryuji Yokokawa, Cheng Ma
-Department of Micro Engineering, Kyoto University, Kyoto 615-8540, Japan
Toshikazu Araoka
-Center for iPS Cell Research and Application (CiRA), Kyoto University, Kyoto 606-8507, Japan
Minoru Takasato
-RIKEN Center for Biosystems Dynamics Research (BDR), Kobe 650-0047, Japan
-Graduate School of Medicine, Osaka University, Suita 565-0871, Japan
-Graduate School of Biostudies, Kyoto University, Kyoto 606-8501, Japan
Paper details:
Cheng Ma, Ramin Banan Sadeghian, Ryosuke Negoro, Kazuya Fujimoto, Toshikazu Araoka , Naoki Ishiguro, Minoru Takasato, Ryuji Yokokawa
Protocol to develop a proximal tubule-on-chip model based on hiPSC-derived kidney organoids for functional analysis of renal transporters
STAR Protocols, Volume 6, Issue 2, 2025, 103777, ISSN 2666-1667
https://doi.org/10.1016/j.xpro.2025.103777
熊本大学ホームページにプレスリリースが掲載されました。
https://www.kumamoto-u.ac.jp/whatsnew/seimei-sentankenkyu/copy_of_20150205
熊本大学 発生医学研究所 腎臓発生分野
理化学研究所 生命機能科学研究センター ヒト器官形成研究チーム
京都大学 大学院工学研究科 マイクロエンジニアリング専攻
東京慈恵会医科大学附属病院 腎臓・高血圧内科
*本国際先導研究で雇用
Support for young researchers mainly includes:
1. Employment as a research fellow or research assistant
2. Independent research funding support
3. Travel expense support
4. Collaborative research support
5. Paper publication support
Additionally, the details of the support and research achievements will be published on the website as part of the international leading research accomplishments. Since achieving as many results as possible from the project will lead to future support, please be sure to submit reports.
【1. Employment as Research Fellow or Research Assistant】
Promising young researchers will be employed as research fellows (postdoctoral researchers) or research assistants (graduate students). For details, please contact the responsible co-investigator.
【2. Independent Research Funding Support】
Each year, when young researchers submit a research plan, those will be reviewed by five domestic principal and co-investigators. Research funds will be provided for outstanding research plans (details here). Young researchers who are not employed in this project are also eligible to apply. The funding limit is 1,000,000 yen for postdoctoral researchers and 300,000 yen for graduate students. They are expected to gain experience in managing research funds independently. At the end of each year, a report (template available here) must be submitted. Both applications and reports should be submitted to the URL below.
https://prsf.kumamoto-u.ac.jp/public/K8pVQwwHfCLeiTb6ogGIc-SsNeQH-SBsZiTFQIcOxUca
【3. Travel Expense Support】
Travel expenses will be supported for domestic and international travels related to collaborative research or conference participation in connection with this international leading research project. For details, please contact the responsible co-investigator. After completing the travel, please be sure to submit a report (template available here) to the URL below.
https://prsf.kumamoto-u.ac.jp/public/X8JWQ0pHfCL7LTZYPcSbHw8PRNCGdAGluo31sohdNkpq
【4. Collaborative Research Support】
To promote domestic collaborative research, the following support systems are available. Travel expenses will be covered by the international leading research project. And consumables should be discussed with the host institution.
• Institute of Molecular Embryology and Genetics, Kumamoto University (Contact: Nishinakamura, Tanigawa)
https://www.imeg.kumamoto-u.ac.jp/kyoten/
• Kyoto University Nanotechnology Hub (Contact: Yokokawa)
http://www.mnhub.cpier.kyoto-u.ac.jp/
• RIKEN (Contact: Takasato)
https://www.bdr.riken.jp/ja/index.html
【5. Paper Publication Support】
Open access publication is encouraged, and the budget for this international leading research can be used for publication fees (APC: Article Processing Charge). If support is received, please submit the funding amount and paper details (authors, title, journal name, pages, year, journal URL, or DOI. Underline the names of co-researchers within this international leading research project) to the URL below (format is flexible).
https://prsf.kumamoto-u.ac.jp/public/785VQHYHvCLkUDd0Z1OY0iG-1X4249nEXd7hQVaypuZO
【Acknowledgment in Paper Publication】
When publishing research outcomes by the support of this international leading research project, please include a statement in the Acknowledgement section or the designated section indicating that the research was conducted with the grant provided. For English papers, include: “JSPS KAKENHI Grant Number JP24K23941”.
For Japanese papers, include: “JSPS 科研費 JP24K23941”.
〈Example〉
【English】This work was supported by JSPS KAKENHI Grant Number JP24K23941 (International Leading Research: Creating a kidney).
【Japanese】本研究は JSPS 科研費 JP24K23941(国際先導研究:腎臓を創る) の助成を受けたものです。
【Reporting All Research Achievements】
Research achievements will be announced on the website of this international leading research project. Please submit the following information in both Japanese and English to the URL below:
• Summary of the achievement (approximately 100 characters in Japanese / 50 words in English).
• When an achievement is generated by collaborative research within this international leading research project, please include the names and affiliations of all co-researchers.
• Summary of conference or workshop presentations (presenter’s name and summary of content).
• When a press release is issued by your affiliated institution, please provide the URL of the press release page.
• When a paper is published, please provide the author(s), title, journal name, pages, year, corresponding journal URL, or DOI. Underline the names of co-researchers within this international leading research project.
https://prsf.kumamoto-u.ac.jp/public/L8ZUQMuH_AL0UFo8ripGHpfA7DyEtOhRnWwvt5_ihzLb