多面的モデルを用いたARPKD嚢胞形成におけるRAC1–SPTAN1の役割解明
Shohei Kuraoka, Yuhei Higashi, Suguru Saito, Solmaz Pourgonabadi, Honami Honjoh, Sho Ishigaki, Peter C. Harris, Lisa M. Satlin, Michifumi Yamashita, Ryuji Morizane. Deciphering the Impact of RAC1-SPTAN1 in ARPKD Cystogenesis Using Multifaceted Models. Advanced Science, (2026)
doi:https://doi.org/10.1002/advs.202524001
[概要説明]
常染色体潜性多発性嚢胞腎(autosomal recessive polycystic kidney disease: ARPKD)は、胎児期からの腎腫大および遠位ネフロン領域に生じる嚢胞形成を主徴とする遺伝性腎疾患であり、現在のところ確立された治療法は存在しません。今回、森實研究室の倉岡将平研究員らは、腎臓オルガノイドモデル(Organoid-on-chip)、遺伝子改変マウス、ヒト腎臓組織を組み合わせた多面的解析により、細胞骨格タンパク質であるSPTAN1が、ARPKDにおける嚢胞形成の重要な制御因子であることを明らかにしました。SPTAN1の低下は、RAC1/c-FOS経路の活性化および細胞内カルシウム濃度の上昇を引き起こし、遠位ネフロンにおける嚢胞形成に寄与していました。さらに、ARPKDモデル腎臓オルガノイドにおいてSPTAN1発現を回復させることで、嚢胞形成が抑制されることを示しました。
本研究は、ARPKDの嚢胞形成に関する新たな分子メカニズムを提示するとともに、SPTAN1がエピゲノム編集を含む新規治療戦略の有望な標的となり得ることを示すものです。
本研究成果は、科学雑誌「Advanced Science」のオンライン版に2026年2月26日に掲載されました。
*倉岡将平研究員は2020年に熊本大学発生医学研究所 腎臓発生分野(西中村隆一教授)で博士課程を修了後、2023年4月から2025年3月までMassachusetts General Hospital(Nephrology Division、森實隆司教授)にて博士研究員として研究に従事しました。現在は熊本大学小児科で小児腎臓を専門に勤務しています。
[背景]
ARPKDは主にPKHD1遺伝子変異により発症する希少な遺伝性腎疾患で、胎児期から進行する遠位ネフロン領域の嚢胞形成により腎腫大を来し、約10%の症例が生後1年以内に腎不全に至ります。嚢胞形成の詳細なメカニズムは未解明であり、根本的な治療法は確立されていません。これまでPKHD1変異マウスや腎臓オルガノイドを用いた研究が行われてきましたが、遠位ネフロンにおける嚢胞形成の再現は困難であり、ARPKD研究における大きな課題となっていました。
2022年にMassachusetts General Hospitalの森實隆司教授らは、流体刺激を付加した腎臓オルガノイドモデル(Organoid-on-chip)を構築し、ARPKD患者の腎病態の再現に成功するとともに、PKHD1欠損に伴うRAC1/c-FOS経路の異常活性化が嚢胞形成に関与することを報告しました(Science Advances, 2022)。しかし、RAC1活性化のメカニズムや嚢胞上皮の細胞起源については未解明でした。
[研究の内容]
本研究では、ヒト腎臓オルガノイド(Organoid-on-chipモデル)、遺伝子改変マウス、ARPKD患者腎組織を用いた多面的解析を行いました。PKHD1ホモ変異を有する多能性幹細胞から腎臓オルガノイドを誘導し、Organoid-on-chipモデルを適用することで、遠位ネフロン特異的な嚢胞形成の再現に成功しました。RNA-seq解析の結果、PKHD1ホモ変異ではRAC1の相互作用分子であるSPTAN1の発現が低下していることが明らかとなりました。また、ARPKD患者の嚢胞上皮においてもSPTAN1の低下が確認されました。
さらに、SPTAN1ヘテロ変異を導入した多能性幹細胞由来オルガノイドでは、遠位ネフロン特異的な嚢胞形成およびRAC1/c-FOS経路の異常活性化が認められ、PKHD1変異と同様の病態が再現されました。この表現型はRAC1阻害剤により抑制されました。加えて、Sptan1ヘテロ変異マウスにおいても、遠位ネフロンの嚢胞形成、腎腫大、およびRAC1活性化が認められました。
また、SPTAN1変異オルガノイドのRNA-seq解析ではカルシウムシグナル関連遺伝子の変動が認められ、実際に嚢胞上皮細胞において細胞内カルシウム濃度の上昇が確認されました。
最後に、PKHD1ホモ変異オルガノイドにおいてSPTAN1発現を回復させることで、嚢胞形成の抑制、RAC1/c-FOS活性の正常化、細胞内カルシウム濃度の是正が達成されました。
[成果・展開]
本研究により、SPTAN1低下を起点としたRAC1/c-FOS経路の異常活性化が、ARPKDにおける嚢胞形成の新たな分子機構であることが示されました。
さらに、ヒト腎組織のsingle-cell RNA-seq解析およびオルガノイド解析から、ARPKDの嚢胞はSLC8A1を発現するconnecting tubule(遠位尿細管と集合管の接続部)に由来する可能性が示唆されました。
本研究は、腎臓オルガノイド、動物モデル、ヒト組織を統合した多面的解析によりこれらの知見を裏付けたものであり、ARPKDの病態解明に大きく貢献する成果です。特に、SPTAN1の関与を示した初めての報告であり、嚢胞性腎疾患に対する新たな治療標的としての可能性を提示しました。今後、ARPKDに対する根本的治療の開発への応用が期待されます。
[用語解説]
・ARPKD:常染色体潜性多発性嚢胞腎。主にPKHD1遺伝子変異により発症する重篤な小児腎疾患。
・遠位ネフロン:腎臓の機能単位であるネフロンのうち、遠位尿細管から集合管までを含む領域。
・Organoid-on-chipモデル:腎臓オルガノイドをマイクロ流体デバイス上に置き、培地を流しながら培養するモデル。オルガノイドに対して流れによる機械刺激を与える。
・SPTAN1:細胞骨格を構成するスペクトリンタンパク質の一つで、細胞構造やシグナル伝達に関与する。
・RAC1:細胞骨格や細胞増殖を制御する低分子GTP結合タンパク質。
・c-FOS:細胞増殖やストレス応答に関与する転写因子。
・SLC8A1:Na/Ca交換輸送体で、細胞内カルシウム調節に重要な役割を持つ。
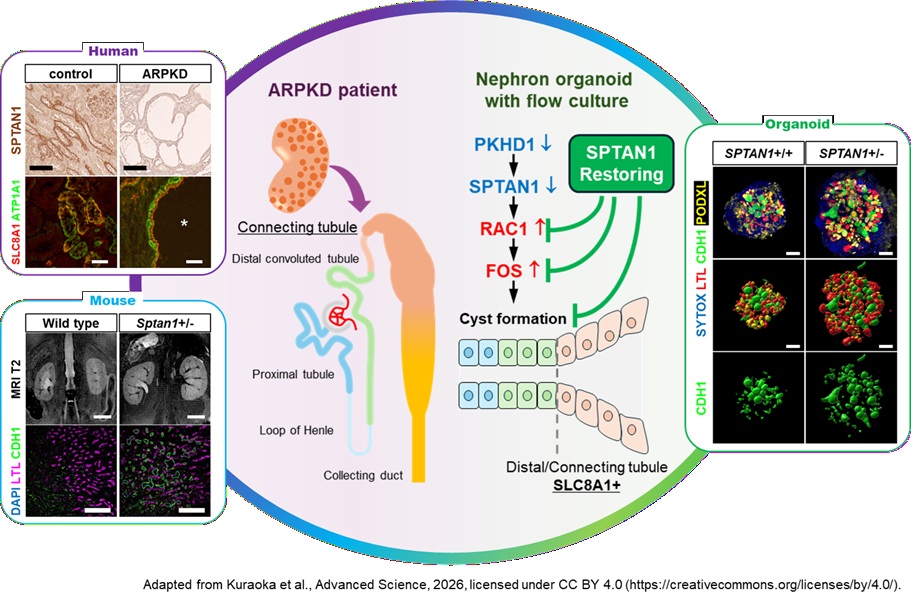
[図の説明]
PKHD1変異は、SPTAN1の低下を起点としてRAC1/c-FOS経路の活性化を引き起こし、嚢胞形成に至る。また、ARPKDの嚢胞はSLC8A1を発現するconnecting tubule(遠位尿細管と集合管の接続部)に由来する可能性が示唆された。これらの知見は、腎臓オルガノイド、遺伝子改変マウス、およびヒト腎組織を統合した多面的解析により明らかとなった。